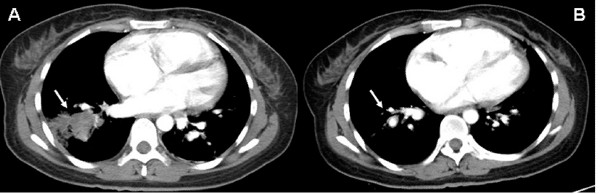
图2.患者胸部CT变化(A 右肺下叶大片实变影,B 治疗后右肺下叶实变影完全消失)
讨论
IE是心脏内膜表面的微生物感染,伴赘生物形成,瓣膜为最常受累部位,但也可发生在间隔缺损部位、腱索或心壁内膜。IE的发病与血液动力学因素导致的心内膜损伤密切相关,约3/4的IE患者有基础性心脏病。血流经病变瓣口或先天性缺损从高压腔至低压腔产生高速射流或湍流,赘生物常位于这些高速射流或湍流下游,如二尖瓣关闭不全的瓣叶心房面、主动脉瓣关闭不全的瓣叶心室面和室间隔缺损的间隔右心室侧,这些湍流下游部位受血流冲击作用损伤,有利于微生物沉积和生长。由于右心系统血流缓慢且右心室压力较左心室低,血流对心内膜的冲击作用较弱,故右心IE(right-sided infective endocarditis,RIE)相对少见,仅占IE总数的5%~10%,主要见有吸毒或静脉药物滥用者,也可见于近期行侵入性心血管操作的患者,如右心导管、中心静脉置管、永久起搏器植入术等,还可见于免疫缺陷或长期使用免疫抑制剂的患者。单纯房间隔缺损患者罹患IE的风险略有升高,若合并其他瓣膜疾病或先天性缺损,IE发病风险显著增加。该患者起病前的外伤史应是导致感染性心内膜炎的主要原因,因金黄色葡萄球菌可引起正常瓣膜的IE,所以推测房间隔缺损可能是导致该患者发病的诱因之一。RIE最常累及三尖瓣,其次为肺动脉瓣与三尖瓣同时受累,孤立性肺动脉瓣IE(isolated pulmonary valve infective endocarditis,IPVIE)极为罕见,而在IPVIE基础上出现PE并发症的病例国内外均未见文献报道。该患者在心房水平存在的左向右分流可引起右心扩大及三尖瓣相对性关闭不全,左向右分流还可引起肺动脉高压及肺动脉瓣相对性关闭不全,在侵袭性和黏附力均较强的金黄色葡萄球菌感染时容易发生IE,因此推测房间隔缺损是间接致病诱因,赘生物部位不在房间隔缺损部而在肺动脉瓣可能与血液动力学因素有关。
赘生物脱落导致的动脉栓塞是IE常见并发症,文献报道临床发生率为20%~40%,尸检检出的亚临床型栓塞可能更多。左心IE(left-sided infective endocarditis,LIE)主要引起脑、心脏、脾、肾、肠系膜和四肢等体循环动脉栓塞,而RIE及伴有左向右分流的LIE,常引起PE。D-二聚体升高对识别肺动脉血栓栓塞有较高的敏感度和特异度,但对赘生物脱落所致化脓性肺栓塞(septic pulmonary embolism)的诊断价值不明确,应定期行经胸超声心动图筛查。如患者在治疗过程中突然出现咳嗽、呼吸困难、咯血或胸痛,应高度怀疑PE,肺动脉CT或造影检查有助于及早明确诊断。
根据2009年欧洲心脏病学学会(ESC)制定的IE防治指南建议,IE早期外科干预的适应证主要包括心力衰竭、感染不能控制及预防栓塞。早期手术按其实施的时间可分为急诊(24小时内)、次急诊(几天内)和择期手术(抗生素治疗1~2周后)。早期手术旨在通过切除感染物、引流脓肿和修复受损组织,避免心力衰竭进行性加重和不可逆性的结构破坏,预防栓塞事件。但在疾病活动期进行手术的风险很大,因此须严格掌握适应证,尽早请心外科医师会诊,为患者确定最佳治疗方案。该患者在治疗过程中并没有出现心力衰竭,而且按照血培养和药敏试验结果选用针对性的抗生素治疗后,感染得到有效控制,因此外科会诊认为没有早期手术指证。患者最终还是发生了化脓性PE,尽管该患者应用抗生素治疗后效果良好,但考虑到PE是一种致死率较高的疾病,因此,是否需要对IE外科治疗指征适当放宽有待进一步探讨。
既往的指南和临床实践均倡导通过预防性使用抗生素来预防IE,这种做法的理论依据是一过性菌血症可引发IE,特别是对于有易患因素的患者。另外,预防性使用抗生素能通过减少或避免菌血症或通过改变细菌的特性,使之不易粘附于内皮表面,从而预防IE。但是上述预防策略的有效性并未在临床试验中得到证实。为了避免过度和无证据使用抗生素,2009年ESC指南一方面继续认可易患IE者在接受医学操作时需要考虑预防性使用抗生素的原则;另一方面,应该将使用抗生素的适应证严格限制在最高危患者。但在临床工作中,完全按照指南来做可能不现实。首先,新的建议颠覆了多年来的临床实践,各专业的各级临床医生、患者、患者家属甚至整个社会都需要为此转换概念。在没有充分证据的情况下,让绝大多数瓣膜性心脏病和先天性心脏病患者在有IE风险时不使用抗生素,医生可能会心里不安,患者们可能会不满意,甚至怀疑医生没有尽责。指南不排除医生因不使用抗生素预防而造成的医疗纠纷甚至诉讼的可能性,但也同时指出不必为此担心,因为遵循指南能够得到法律保护。但这不符合我国国情,因为欧洲国家处理医疗纠纷时不要求医务人员"举证责任倒置"。



 京公网安备 11010502033353号
京公网安备 11010502033353号